I. KHÁI NIỆM, ĐỒNG PHÂN, DANH PHÁP
- Ankin là hiđrocacbon không no, mạch hở trong phân tử có chứa 1 liên kết ba CΞC còn lại là các liên kết đơn.
- Công thức tổng quát của ankin: CnH2n-2 (n ≥ 2).
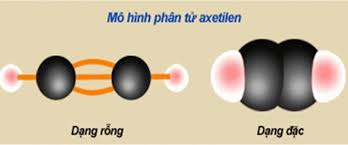
Ankin đơn giản nhất - C2H2 (axetilen)
- Tên gọi:
+ Tên thay thế:
Số chỉ vị trí mạch nhánh + tên nhánh + tên mạch chính + số chỉ vị trí nối ba + in
+ Tên thường:
Tên gốc hiđrocacbon gắn với C mang liên kết ba + axetilen
- Ankin có các loại đồng phân: đồng phân bixicloankan (n ≥ 4), đồng phân vị trí liên kết ba (n ≥ 4); đồng phân mạch C (n ≥ 5); đồng phân xicloanken, đồng phân ankađien.
II. TÍNH CHẤT HOÁ HỌC
1. Phản ứng cộng
a. Cộng H2
CnH2n-2 + H2 → CnH2n (Pd/PbCO3, t0)
CnH2n-2 + 2H2 → CnH2n+2 (Ni, t0)
Chú ý:
- Tuỳ thuộc vào xúc tác được sử dụng mà phản ứng cộng H2 vào ankin xảy ra theo các hướng khác nhau.
- Thường thì phản ứng cộng H2 vào ankin thường tạo ra hỗn hợp gồm nhiều sản phẩm.
- Số mol khí giảm = số mol H2 tham gia phản ứng. Chú ý bảo toàn khối lượng, bảo toàn H, bảo toàn C.
b. Cộng Br2
CnH2n-2 + Br2 → CnH2n-2Br2
CnH2n-2 + 2Br2 → CnH2n-2Br4
Khối lượng dung dịch brom tăng chính là khối lượng ankin đã phản ứng.
c. Cộng HX
- Cộng H2O:
+ C2H2 → anđehit
CHΞCH + H2O → CH3 - CHO (H2SO4, HgSO4, 800C)
+ Ankin khác → xeton
CHΞC-CH3 + H2O → CH3-CO-CH3 (H+)
- Cộng axit:
CHΞCH + HCl → CH2=CHCl (vinyl clorua) (Hg2Cl2 ở 150 đến 2000C)
CHΞCH + HCN → CH2=CH-CN (nitrin acrylic)
CHΞCH + CH3COOH → CH3COOCH=CH2 (vinylaxetat)
CHΞCH + C2H5OH → CH2=CH-O-CH3 (etylvinylete)
2. Phản ứng trùng hợp
- Đime hóa
2CHΞCH → CHΞC-CH=CH2 (vinyl axetilen) (NH4Cl, Cu2Cl2, t0)
- Trime hóa
3CHΞCH → C6H6 (C, 6000C)
- Trùng hợp (polime hóa)
nCHΞCH → (-CH=CH-)n (xt, t0, p) (nhựa cupren)
3. Phản ứng oxi hóa
a. Phản ứng oxi hóa hoàn toàn
CnH2n-2 + (3n - 1)/2O2 → nCO2 + (n - 1)H2O
→ đặc điểm của phản ứng đốt cháy ankin: nCO2 > nH2O và nCO2 - nH2O = nankin.
b. Phản ứng oxi hóa không hoàn toàn
- Các ankin đều làm mất màu dung dịch thuốc tím ở nhiệt độ thường.
3C2H2 + 8KMnO4 + 2H2O → 3(COOK)2 + 2MnO2 + 2KOH
Nếu trong môi trường axit thì tạo thành CO2 sau đó CO2 phản ứng với KOH tạo thành muối.
- Với các ankin khác sẽ có sự đứt mạch tạo thành hỗn hợp 2 muối.
R1-CΞC-R2 + 2KMnO4 → R1COOK + R2COOK + 2MnO2
4. Phản ứng thế của ank-1-in
CHΞCH + Ag2O → CAgΞCAg↓ + H2O
2CHΞC-R + Ag2O → CAgΞC-R↓ (vàng) + H2O
Chú ý:
- Chỉ có C2H2 mới phản ứng với Ag2O theo tỉ lệ mol 1:1; các ank-1-in khác chỉ phản ứng theo tỉ lệ 2:1.
- Nếu có hỗn hợp ankin tham gia phản ứng với Ag2O mà tỉ lệ mol của (ankin : Ag2O) = k có giá trị:
+ k < 2 → có C2H2.
+ k > 2 → không có C2H2
+ k = 2 → hỗn hợp gồm 2 ank-1-in hoặc hỗn hợp C2H2 và ankin khác (không phải ank-1-in) có số mol bằng nhau.
- Từ kết tủa vàng thu được có thể khôi phục lại ankin ban đầu bằng cách cho tác dụng với HCl.
CAgΞC-R + HCl → CHΞC-R + AgCl
(phản ứng này dùng để tách ank-1-in khỏi hỗn hợp)
- Ngoài cách viết với Ag2O có thể viết phản ứng với dung dịch AgNO3/NH3 và phản ứng này được dùng để nhận biết ank-1-in.
III. ĐIỀU CHẾ AXETILEN
- Nhiệt phân metan:
2CH4 → C2H2 + 3H2 (15000C, làm lạnh nhanh)
- Thủy phân CaC2: (có trong đất đèn)
CaC2 + 2H2O → Ca(OH)2 + C2H2
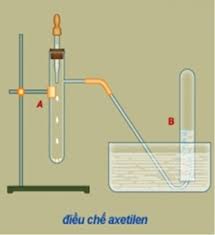
Điều chế axetilen bằng phản ứng thủy phân CaC2
Bài viết liên quan:


Làm bài thử