I. Nước là chất điện li yếu
1. Sự điện li của nước
Nước điện li rất yếu theo phương trình sau: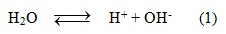
2. Tích số ion của nước
Vậy môi trường trung tính là môi trường có:[H+] = [OH-]
Tại 250C, trong nước nguyên chất có:
[H+] = [OH-] = 1,0.10-17 M.
Đặt: KH2O = [H+] . [OH-] = 1,0.10-17 . 1,0.10-17 = 1,0.10-14
KH2O được gọi tích số ion của nước.
Ở nhiệt độ xác định, tích số này là hằng số không những trong nước tinh khiết mà cả trong những dung dịch loãng khác nữa.
3. Ý nghĩa tích số ion của nước
a. Môi trường axit
Khi cho axit HCl vào nước, nồng độ H+ tăng, mà tích số ion trong nước không đổi nên nồng độ OH- phải giảm.Ví dụ: Hòa tan HCl vào nước để được [H+] = 1,0.10-3M =>[OH-] = 1,0.10-11M
Vậy môi trường axit là môi trường có:
[H+] > [OH-] hay [H+] > 1,0.10-7M
b. Môi trường kiềm
Khi cho NaOH vào nước, nồng độ OH- tăng, mà tích số ion trong nước không đổi nên nồng độ H+ phải giảm.Vậy môi trường kiềm là môi trường có:
[H+] < [OH-] hay [H+] < 1,0.10-7M
Kết luận:
- Môi trường trung tính: [H+] > 1,0.10-7M
- Môi trường axit: [H+] < 1,0.10-7M
- Môi trường kiềm: [H+] → 1,0.10-7M
II. Khái niệm pH, chất chỉ thị axit – bazơ
1. Khái niệm về pH
Để đánh giá độ kiềm, độ axit của dung dịch có thể dựa vào [H+].Để tránh ghi giá trị [H+] với số mũ âm, người ta dùng gía trị pH với quy ước:
pH = - lg[H+] ; [H+] = 10- pH
Ta có:- pH = 7 môi trường trung tính.
- pH < 7 môi trường axit.
- pH > 7 môi trường kiềm.
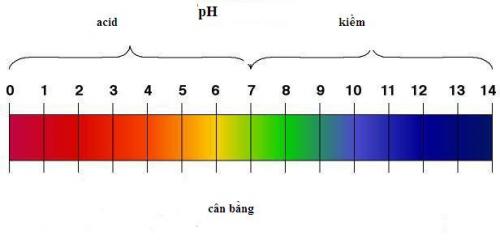
Thang pH thường dùng có giá trị từ 1 đến 14.
2. Chất chỉ thị axit – bazơ
Chất chỉ thị axit – bazơ là chất có màu biến đổi phụ thuộc theo giá trị pH của dung dịch.Khi trộn lẫn một số chất chỉ thị axit – bazơ có màu biến đổi kế tiếp nhau theo giá trị pH ta thu được chất chỉ thị vạn năng.
Bài viết liên quan:


Nước thuộc môi trường nào ?tại sao