Điện ly là một phần kiến thức rất hay trong chương trình hóa học lớp 11. Nó có vai trò rất quan trọng trong việc giải thích nhiều hiện tượng của hóa học vô cơ. Tuy nhiên, vẫn còn nhiều tranh cãi về vấn đề này. Vì vậy, trong bài này, ngoài việc nói về cơ chế của sự phân ly của thành các ion của các phần tử khi tan trong dung môi phân cực hoặc bị nóng chảy, mình cũng đưa ra những vấn đề đang được tranh luận để các bạn có thể tham khảo. Trước tiên là cơ chế của sự điện ly…
Xét một phân tử muối ăn NaCl, khi ta bỏ vào trong nước thì NaCl có tan một chút it, nhưng vẫn còn phần chưa tan lắng lại. Chúng ta ai cũng biết là khi khuấy lên, chắc chắn thì lượng NaCl sẽ tan hết, nhưng tại sao lại như vậy? Nếu bạn không giải thích được thì có nghĩa là bạn mới chỉ nắm được cái hiện tượng, cái bề mặt chứ chưa đi vào bản chất của sự việc.
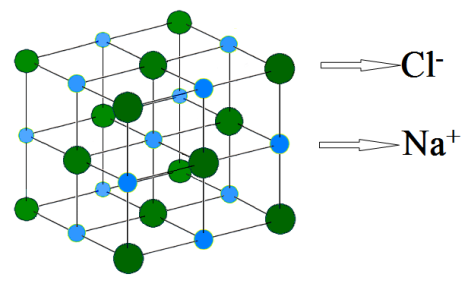
Giải thích vấn đề này không khó. Phân tử NaCl là hợp chất có liên kết ion, và chúng có mạng tinh thể như ở hình vẽ phía dưới. Ở mỗi nút mạng là một ion Na+ hoặc Cl-, những ion âm – dương này xen kẽ nhau.
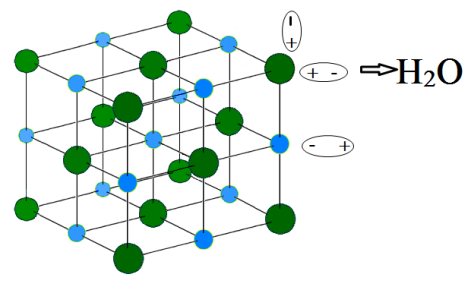
Khi ta thả muối ăn vào nước, một lượng nhỏ bị tan vào dung dịch. Lượng còn lại vẫn nằm ở đáy cốc, không tan. Tuy nhiên, chúng được sự “quan tâm chăm sóc” rất đặc biệt của các phân tử H2O như hình vẽ phía dưới. Vì các phân tử H2O phân cực nên đầu âm của H2O sẽ hút các ion dương Na+ thông qua lực hút tĩnh điện, và tương tự đầu âm của H2O cũng sẽ hút các ion Cl-.
Như vậy khối NaCl hoàn toàn bị “bao vây” bởi “đội quân H2O” của bạn. Bây giờ bạn chỉ cần ra “chỉ thị” bằng cách khuấy mạnh nước trong cốc. Lập tức, các phân tử nước sẽ chạy nhặng lên nhưng nhất quyết không chịu buông các ion Na+ và Cl- ra. Giằng co một lúc, các ion Na+ và Cl- không còn đủ sức liên kết với nhau nữa đành buông tay nhau ra, biến thành các ion đi vào trong dung dịch. Vậy là NaCl đã tan và phân ly thành ion. Đến đây chúng ta có một vài lưu ý sau :
Thứ nhất, thường thì chỉ những phân tử có liên kết ion mới có khả năng phân ly thành các ion âm – dương (hiện tượng này gọi là điện ly).
Thứ hai, dung môi phải là dung môi phân cực thì sự điện ly mới xảy ra. Nếu như ở ví dụ trên mà bạn hòa NaCl vào dầu hỏa thì bạn cứ ngồi mà khuấy đến sáng mai nó cũng chẳng chịu tan cho bạn tẹo nào. Vì cái đội quân dầu hỏa là cái đội quân “vô trách nhiệm”. Chúng không phân cực nên dĩ nhiên không có đầu âm – dương để “quan tâm” tới các ion Na+ và Cl-. Và như thế khi bạn ra “chỉ thị” thì chúng cũng vẫn chạy nhặng lên, nhưng rút cục chả kéo được thằng Na+ hay Cl- nào ra cả.
Thứ ba, dung dịch càng loãng thì độ điện ly càng tăng. Độ điện ly alpha (α) được định nghĩa bằng tỷ số giữa tổng số các phân tử đã phân ly trên tổng số các phân tử đã tan α = nphân ly /ntan . Như vậy cùng một lượng chất đã tan càng phân ly ra nhiều ion thì độ điện ly càng mạnh. Dung dịch mà càng loãng thì rõ ràng số phân tử H2O đến “quan tâm” tới mỗi ion trong mạng NaCl sẽ nhiều lên, và như thế việc lôi chúng ra sẽ dễ dàng hơn. Vì vậy chúng sẽ phân ly nhiều hơn. Tuy nhiên, đối với những chất điện ly mạnh thì điều này không quan trọng, vì bản chất chúng rất “yếu đuối”, chỉ cần một thằng H2O đến dọa một cái là chúng đã sợ vỡ mật, ngoan ngoãn nghe theo rồi. Rắn mặt hơn thì phải, nói đến mấy thằng ít tan như BaSO4 , AgCl, CuS,…. bọn này phải tốn công tốn sức hơn, nhưng cũng chỉ lôi cổ được vài thằng ra, còn lại bọn chúng vẫn cứ nhơn nhơn cái mặt ra, không có cách gì làm chúng khuất phục được. Mà dạo này lại đang rộ lên mấy cái tranh cãi là BaSO4 và AgCl có phải là chất điện ly mạnh hay không? Nói đúng cũng phải mà không đúng cũng chẳng sai. Chỉ tại các bác trên Bộ mỗi người định nghĩa một kiểu, người nào cũng muốn bảo vệ “chính kiến” của mình nên chẳng ai chịu nhường ai, như hai con dê đen và dê trắng đi chung một chiêc cầu vậy. Chỉ khác cái là trong chuyện, hai con dê húc nhau rồi rơi xuống suối, đằng này vô duyên vô cớ học sinh bị lôi vào làm con ruồi ở giữa. Sau trận ẩu đả, con ruồi chết, còn hai con dê vẫn chả sao, haizzz…… Sự tình cụ thể là thế này, nhóm các bác theo phe “cánh tả” thì đồng tình với quan điểm như mình đã nêu trên, nghĩa là: Độ điện ly alpha (α) được định nghĩa bằng tỷ số giữa tổng số các phân tử đã phân ly trên tổng số các phân tử đã tan α = nphân ly /ntan . Tức là dù nó tan ít, nhưng cái chỗ đã tan ấy mà nó phân ly gần hết thành ion thì nó vẫn được coi là điện ly mạnh. Nói như thế thì nghiễm nhiên hai thằng rắn mặt BaSO4 và AgCl được ra nhập danh sách những chất chất điện ly mạnh. Tuy nhiên, các bác ở phe “cánh hữu” lại cho rằng việc này không thể chấp nhận được. Giống như một thằng học sinh cả năm học vừa ngu vừa dốt, không làm ra cái trò trống gì ra hồn, chỉ vì cuối kỳ nó được 9, 10 điểm mà xét nó là học sinh giỏi thì vô lý quá. Muốn xem nó giỏi hay dốt thì phải xét kết quả cả năm chứ. Vì vậy các bác bên cánh hữu ủng hộ quan điểm, phải xét thêm quá trình nó tan trước đã rồi mới tính đến định nghĩa trên, nếu mà xét thế thì hai thằng rắn mặt kia trăm phần trăm bị loại khỏi danh sách điện ly mạnh. Mỗi người một ý rồi không thống nhất được quan điểm, chỉ chết học sinh thôi. Haizzz…
Tạm gác lại cái vụ tranh cãi bên trên bây giờ mình sẽ giải thích là tại sao ngoài điện ly trong dung môi phân cực ra thì các chất lại có thể điện ly khi nóng chảy. Khi nóng chảy, do nhiệt độ quá cao nên các phân tử chất điện ly dao động nhiệt rất mạnh, vì vậy chúng không thể giữ liên lạc với nhau được nữa, đành phải buông tay nhau ra, thế là nó chảy lỏng. Kế đến, ngay bản thân phân tử chất điện ly, sau khi chia tay các đồng đội cũng không thể chịu đựng được nữa đành phân ly tiếp thành các ion. Đó là nguyên nhân làm các chất điện ly khi nóng chảy.
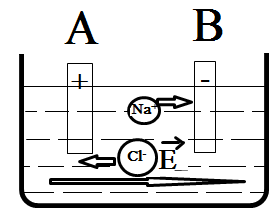
Bây giờ mình sẽ nói nốt vấn đề do đâu mà dung dịch chất điện ly có thể dẫn điện được. Điều này đơn giản là vì các cation va anion chất điện ly sau khi đã phân ly trong dung dịch nó sẽ đi “lang thang linh tinh”. Do bản chất nó là ion chứ không phải phân tử trung hòa nên rất thích hợp đóng vai trò “vật tải điện”. Để hiểu rõ hơn bạn nhìn hình vẽ phía dưới.
Khi ta cắm nguồn 1 chiều vào hai đầu A và B, giả sử A dương – B âm. Lập tức hình thành một điện trường trong dung dịch có chiều hướng từ A sang B. Điện trường này gây ra lực tác dụng lên các ion trong dung dịch, nó sẽ lôi những thằng có điện tích âm về cực dương, và những thằng điện tích dương về cực âm. Như vậy, trong dung hịch hình thành một “dòng ion” đóng vai trò như electron tự do trong kim loại, để dẫn điện.

Ý kiến bạn đọc