I. VỊ TRÍ – CẤU TẠO
1. Vị trí
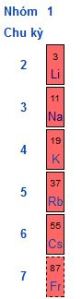 | Các kim loại kiềm thuộc nhóm IA của bảng tuần hoàn các nguyên tố, bao gồm: liti (Li), natri (Na), kali (K), rubiđi (Rb), xesi (Cs) và 1franxi (Fr). Các kim loại nhóm này được gọi là kim loại kiềm vì hidroxit của chúng là chất kiềm mạnh. Franxi là nguyên tố phóng xạ tự nhiên. |

Liti (Li)

Natri (Na)

Kaili (K)

Rubidi (Rb)

Xesi (Cs)
2. Cấu tạo
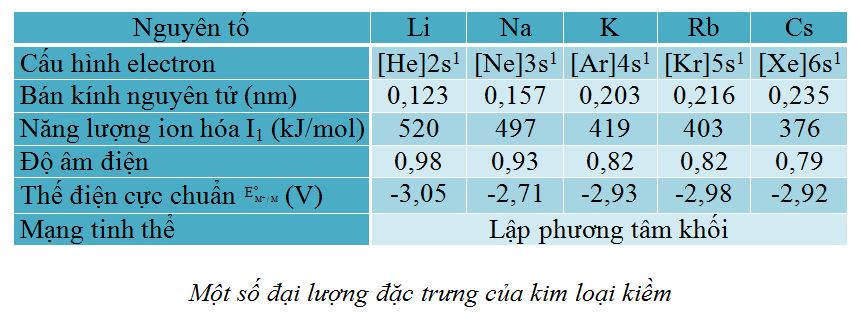
Kim loại kiềm là những nguyên tố s, có một electron lớp ngoài cùng, ở phân lớp ns1 . Đây là electron hóa trị nằm ngoài cấu hình electron bền của các khí hiếm, nên các nguyên tử kim loại kiềm rất dễ mất đi một electron hóa trị biến thành ion dương M+. Vì thế các kim loại kiềm là những kim loại rất hoạt động.
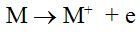
Các cation M+ của kim loại kiềm có cấu hình electron của nguyên tử khí hiếm đứng trước.
Các nguyên tử kim loại kiềm có năng lượng ion hóa thứ nhất nhỏ nhất so với các kim loại khác cùng chu kì. Điều này cũng chứng tỏ độ hoạt động hóa học mạnh của các kim loại kiềm. Tuy vậy, năng lượng ion hóa thứ hai của chúng lại rất lớn so với năng lượng ion hóa thứ nhất, do đó trong các phản ứng hóa học, các nguyên tử kim loại kiềm chỉ nhường đi 1 electron.
Các kim loại kiềm chủ yếu tạo nên các hợp chất ion, trong đó số oxi hóa duy nhất là +1. Tuy nhiên chúng cũng có thể tạo nên liên kết cộng hóa trị trong các phân tử M2 tồn tại ở trạng thái khí.
Các ion của kim loại kiềm không có màu. Các hợp chất của chúng dễ tan trong nước trừ một số hợp chất của liti.

Ý kiến bạn đọc