1. Tác dụng với phi kim
Hầu hết các kim loại kiềm có thể khử được các phi kim.
Với hidro: Khi đun nóng, các kim loại kiềm kết hợp với hidro tạo hidrua ion: Li ở 600-700oC, còn các kim loại kiềm khác ở 350-400oC.
Với oxi:
+ Ở điều kiện thường và trong không khí khô:
Li bị phủ một lớp màu xám gồm Li2O và Li3N.
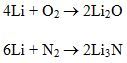
Na bị oxi hóa thành Na2O2 và lẫn một ít Na2O.
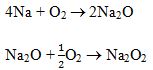
K bị phủ lớp KO2 ở ngoài cùng và bên trong là lớp K2O.
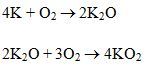
Rb và Cs tự bốc cháy tạo RbO2 và CsO2.
+ Khi đốt nóng: Li tạo Li2O và một ít Li2O2, còn các kim loại kiềm khác, oxit của chúng tác dụng tiếp với oxi tạo peoxit (Na2O2) hoặc supeoxit (KO2, RbO2, CsO2).
Với halogen, lưu huỳnh:
Các kim loại kiềm bốc cháy trong khí clo khi có mặt hơi ẩm ở nhiệt độ cao. Với brom lỏng, K, Rb, Cs nổ mạnh, Li và Na chỉ tương tác trên bề mặt. Với iot, các kim loại kiềm chỉ tương tác mạnh khi đun nóng.
Khi nghiền kim loại kiềm với bột lưu huỳnh sẽ gây phản ứng nổ.
Với nitơ, cacbon, silic:
Chỉ có Li có thể tương tác trực tiếp tạo Li3N, Li2C2, Li6Si2 khi đun nóng.
2. Tác dụng với nước
Các kim loại kiềm có thế điện cực rất âm, vì thế chúng tương tác rất mãnh liệt với nước giải phóng khí hidro.
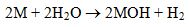
Khi phản ứng với nước, Li không cho ngọn lửa, Na nóng chảy thành hạt tròn nổi và chạy trên mặt nước, hạt lớn có thể bốc cháy, K bốc cháy ngay còn Rb và Cs gây phản ứng nổ.
Do kim loại kiềm hoạt động hóa học mạnh, đặc biệt là bị oxi hóa nhanh trong không khí và có phản ứng mãnh liệt với nước, cần phải bảo quản kim loại kiềm trong dầu hỏa khan, trong chân không hoặc trong khí trơ và thật cẩn thận khi làm thí nghiệm với kim loại kiềm.
3. Tác dụng với axit
Thế điện cực chuẩn của cặp oxi hóa – khử của kim loại kiềm có giá trị từ -3.05V đến -2,71V cho nên các kim loại kiềm có thể khử dễ dàng ion H+ của dung dịch axit thành khí hidro.
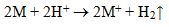
Phản ứng của kim loại kiềm với axit cũng là phản ứng gây nổ nguy hiểm, cần cẩn thận!


Ý kiến bạn đọc