I. ĐỊNH NGHĨA
- Các định nghĩa về amin:
+ Amin là sản phẩm thu được khi thay thế nguyên tử H trong phân tử NH3 bằng các gốc hiđrocacbon. (chỉ đúng với amin đơn chức).
Amoniac
+ Amin là sản phẩm thu được khi thay thế nguyên tử H trong hidrocacbon bằng nhóm -NH2 (chỉ đúng với amin bậc 1).
+ Amin là hợp chất hữu cơ trong phân tử chỉ chứa 3 nguyên tố: C, H và N.
- Bậc của amin là số gốc hiđrocacbon liên kết với nguyên tử N.
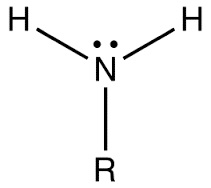
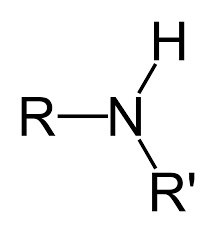
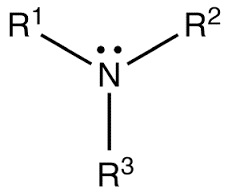
Amin bậc 1 Amin bậc 2 Amin bậc 3
- Công thức tổng quát của amin:
CxHyNz (x, y, z thuộc N*; y ≤ 2x + 2 + z; y chẵn nếu z chẵn; y lẻ nếu z lẻ).
Hoặc CnH2n+2-2k+tNt (n thuộc N*; k thuộc N; t thuộc N*).
Số liên kết pi + số vòng trong phân tử amin = (2x + 2 + t - y)/2.
Nếu là amin bậc I thì công thức tổng quát có thể đặt là: CnH2n+2-2k-t(NH2)t..
II. DANH PHÁP
1. Tên thay thế
Tên amin = Tên của hiđrocacbon tương ứng + Số thứ tự của C chứa nhóm NH2 + amin
2. Tên gốc chức
Tên amin = Gốc hiđrocacbon + amin
3. Tên thường
Anilin…
III. TÍNH CHẤT VẬT LÍ
- Các amin có khả năng tan tốt trong nước. Độ tan trong nước giảm khi số nguyên tử C tăng.
- Giữa amin và nước có liên kết Hiđro liên phân tử
- Metylamin, đimetylamin, trimetylamin và etylamin là chất khí, có mùi khai; các amin còn lại đều tồn tại ở trạng thái lỏng, rắn. Anilin: lỏng, không màu, độc ít tan trong nước dễ bị oxi hóa chuyển thành màu nâu đen.
IV. TÍNH CHẤT HOÁ HỌC
1. Tính bazơ
a. Giải thích tính bazơ của các amin
Do nguyên tử N trong phân tử amin còn cặp e chưa sử dụng có khả năng nhận proton.
b. So sánh tính bazơ của các amin
- Nếu nguyên tử N trong phân tử amin được gắn với gốc đẩy e (gốc no: ankyl) thì tính bazơ của amin mạnh hơn so với tính bazơ của NH3. Những amin này làm cho quỳ tím chuyển thành màu xanh.
- Nếu nguyên tử N trong phân tử amin gắn với các gốc hút e (gốc không no, gốc thơm) thì tính bazơ của amin yếu hơn so với tính bazơ của NH3. Những amin này không làm xanh quỳ tím.
- Amin có càng nhiều gốc đẩy e thì tính bazơ càng mạnh, amin có càng nhiều gốc hút e thì tính bazơ càng yếu.
2. Các phản ứng thể hiện tính bazơ
a. Phản ứng với dung dịch axit
CH3NH2 + H2SO4 → CH3NH3HSO4
2CH3NH2 + H2SO4 → (CH3NH3)2SO4
CH3NH2 + CH3COOH → CH3NH3OOCCH3
b. Phản ứng với dung dịch muối tạo bazơ không tan
2CH3NH2 + MgCl2 + 2H2O → Mg(OH)2 + 2CH3NH3Cl
3. Phản ứng nhận biết bậc của amin
- Nếu là amin bậc I khi phản ứng với HNO2 tạo khí thoát ra:
RNH2 + HNO2 → ROH + N2 + H2O
Anilin phản ứng tạo muối điazoni ở 0 → 50C:
C6H5NH2 + HNO2 → C6H5N2+Cl- + 2H2O
- Nếu là amin bậc II thì tạo hợp chất nitrozo màu vàng nổi trên mặt nước:
RNHR’ + HNO2 → RN(NO)R’ + H2O
- Amin bậc III không có phản ứng này.
4. Phản ứng nâng bậc amin
RNH2 + R’I → RNHR’ + HI
RNHR’ + R’’I → RNR’R’’ + HI
5. Phản ứng riêng của anilin
- Anilin là amin thơm nên không làm đổi màu quỳ tím thành xanh.
- Anilin tạo kết tủa trắng với dung dịch nước Brom:
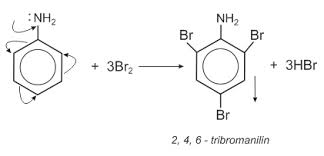
→ Phản ứng này được dùng để nhận biết anilin.
V. ĐIỀU CHẾ
1. Hiđro hóa hợp chất nitro
C6H5NO2 + 6H → C6H5NH2 + 2H2O (Fe/HCl)
2. Dùng kiềm mạnh đẩy amin ra khỏi muối amoni
C6H5NH3Cl + NaOH → C6H5NH2 + NaCl + H2O
→ Phản ứng này dùng để tách anilin ra khỏi hỗn hợp.
3. Thay thế nguyên tử H của NH3 (phản ứng nâng bậc)
NH3 + RI → R - NH2 + HI
Bài viết liên quan:


Ý kiến bạn đọc