I. Sự chuyển động của Electron
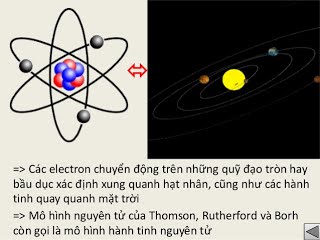
Các electrron chuyển dộng rất nhanh (tốc độ hàng nghìn km/s) trong khu vực xung quanh hạt nhân nguyên tử không theo những quỹ đaọ xác định tạo nên vỏ nguyên tử.
II. Lớp electron và phân lớp electron
1. Lớp e
Các electron trong nguyên tử ở trạng thái cơ bản lần lượt chiếm các mức năng lượng từf thấp đến cao và sắp xếp thành từng lớp. Các electron ở gần nhân liên kết bền hơn với hạt nhân. Vậy electron ở lớp trong có mức năng lượng thấp hơn so với ở các lớp ngoàiCác electron trên cùng 1 lớp có mức năng lượng gần bằng nhau
Xếp theo thứ tự mức năng lượng từ thấp đến cao, các lớp e này được ghi bằng các số nguyên tử theo thứ tự n= 1, 2, 3, 4... với tên gọi : K, L, M,N...
2. Phân lớp electron
Mỗi lớp electron lại chia thành các phân lớpCác electron trên cùng một phân lớp có mức năng lượng bằng nhau
Các phân lớp được kí hiệu bằng các chứ cái thường s, p, d, f
Số phân lớp trong mỗi lớp bằng số thứ tự của lớp đó
III. Số electron tối đa trong một phân lớp, một lớp
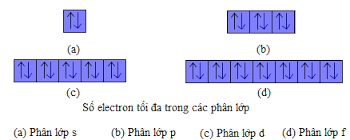
- Phân lớp s chứa tối đa 2 electron
- Phân lớp p chứa tối đa 6 electron
- Phân lớp d chứa tối đa 10 electron
- Phân lớp f chứa tối đa 14 electron
Phân lớp electron đã có đủ số electron tối đa gọi là phân lớp electron bão hòa
Ví dụ:Sơ đò sự phân bố electon trên các lớp của nguyên tử Natri, Silic, germanium
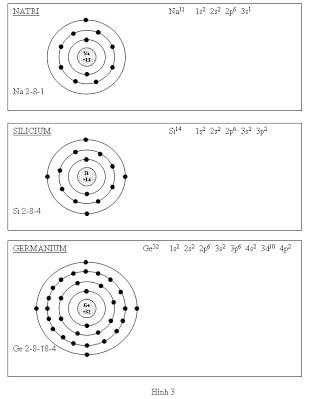

Cách tính số e tối đa của mỗi lớp