I - SỰ HÌNH THÀNH LIÊN KẾT CỘNG HÓA TRỊ BẰNG CẶP ELECTRON CHUNG
1. Sự hình thành phân tử đơn chất
a) Sự hình thành phân tử Hidro H2
H : 1s1 và He : 1s2Sự hình thành phân tử H2 :
Mỗi chấm bên kí hiệu nguyên tố biểu diễn một electron ở lớp ngoài cùng, được gọi là công thức electron. Thay hai chấm bằng gạch, ta có gọi là công thức cấu tạo.Giữa nguyên tử hiđro có cặp electron liên kết biểu thị bằng một gạch , đó là liên kết đơn.
b) Sự hình thành phân tử N2
N : 1s22s22p3Ne : 1s22s22p6
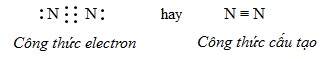
Hai nguyên tử N liên kết với nhau bằng 3 cặp electron liên kết biểu thị bằng 3 gạch ( ≡ ), đó là liên kết 3. Liên kết 3 bền hơn liên kết đôi
c) Khái niệm liên kết cộng hoá trị
ĐN: Liên kết cộng hoá trị là liên kết được tạo nên giữa 2 nguyên tử bằng 1 hay nhiều cặp electron dùng chung
- Mỗi cặp electron chung tạo nên 1 liên kết cộng hoá trị, nên ta có liên kết đơn (trong phân tử H2) , liên kết ba (trong phân tử N2)
- Liên kết trong các phân tử H2 , N2 tạo nên từ 2 nguyên tử của cùng 1 nguyên tố (có độ âm điện như nhau) , do đó liên kết trong các phân tử đó không phân cực . Đó là liên kết cộng hoá trị không phân cực
2. Sự hình thành phân tử hợp chất
a) Sự hình thành phân tử
Trong phân tử hiđro clorua, mỗi nguyên tử góp electron tạo thành cặp electron chung để tạo nên một liên kết cộng hóa trị. Độ âm điện của Clo là lớn hơn độ âm điện của hiđro là nên cặp electron liên kết bị lệch về phía Clo, liên kết cộng hóa trị này bị phân cực.

Liên kết cộng hóa trị trong đó cặp electron chung bị lệch về phía một nguyên tử được gọi là liên kết cộng hóa trị có cực hay liên kết cộng hóa trị phân cực.
b) Sự hình thành phân tử khí cacbonic CO2 (có cấu tạo thẳng)
Cấu hình electron nguyên tử của là , nguyên tử cacbon có electron ở lớp ngoài cùngCấu hình electron nguyên tử của là , nguyên tử oxi có electron ở lớp ngoài cùng
Trong phân tử , nguyên tử nằm giữa nguyên tử và góp chung với mỗi nguyên tử hai electron, mỗi nguyên tử góp chúng với nguyên tử C hai electron tạo ra liên kết đôi.
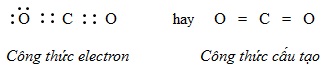
Kết luận : Theo công thức electron, mỗi nguyên tử C hay O đều có 8e ở lớp ngoài cùng đạt cấu hình của khí hiếm nên phân tử CO2 bền vững
c) Liên kết cho - nhận
Trong một số trường hợp, cặp electron chung chỉ do một nguyên tử đóng góp thì liên kết giữa hai nguyên tử là liên kết cho - nhận
3. Tính chất
Các chất mà phân tử chỉ có liên kết cộng hóa trị có thể là chất rắn như đường, lưu huỳnh, iot,..., có thể là chất lỏng: nước, ancol,... hoặc chất khí như khí cacbonic, clo, hiđro,... Các chất có cực như ancol etylic, đường,... tan nhiều trong dung môi có cực như nước. Phần lớn các chất không cực như iot, các chất hữu cơ không cực tan trong dung môi không cực như benzen, cacbon tetraclorua,...Nói chung, các chất chỉ có liên kết cộng hóa trị không cực không dẫn điện ở mọi trạng thái.
II - LIÊN KẾT CỘNG HÓA TRỊ VÀ SỰ XEN PHỦ CÁC OBITAN NGUYÊN TỬ
1. Sự xen phủ của các obitan nguyên tử khi hình thành các phân tử đơn chất
a) Sự hình thành phân tử
Để hình thành liên kết giữa hai nguyên tử trong phân tử hiđro, hai obitan của hai nguyên tử xen phủ với nhau tạo ra vùng xen phủ giữa hai hạt nhân nguyên tử. Xác suất có mặt của các electron tập trung chủ yếu ở khu vực giữa hai hạt nhân.Vì vậy, ngoài lực đẩy tương hỗ giữa hai proton và hai electron còn có lực hút giữa các electron vơi hai hạt nhân hướng về tâm phân tử (hình ). 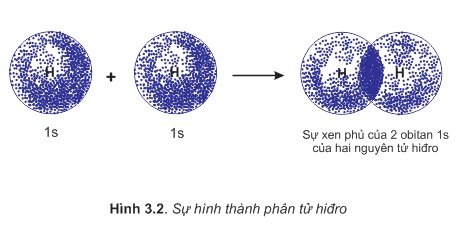
Khi hai hạt nhân có khoảng cách , các lực hút và lực đẩy cân bằng nhau ( được gọi là khoảng cách cân bằng hay độ dài của liên kết ).
Ở khoảng cách cân bằng trên, phân tử có năng lượng thấp hơn tổng năng lượng của hai nguyên tử riêng rẽ.
Đó là nguyên nhân của sự hình thành liên kết cộng hóa trị giữa hai nguyên tử và là một liên kết hóa học bền.
b) Sự hình thành phân tử
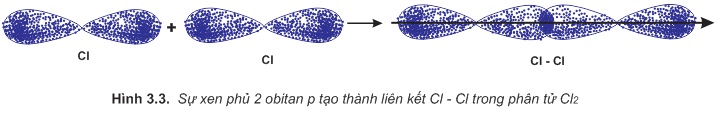
Để giải thích sự hình thành liên kết , có thể dựa vào cấu hình electron của mỗi nguyên tử clo:
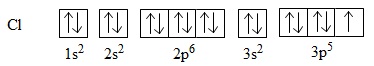
Sự hình thành liên kết giữa hai nguyên tử clo là do sự xen phủ giữa hai obitan p chứa electron độc thân của mỗi nguyên tử clo
.
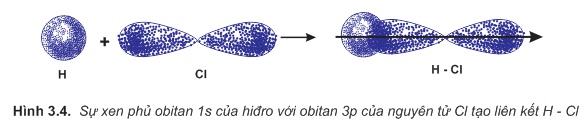
được hình thành nhờ sự xenphủ giữa obitan của nguyên tử hiđro và obitan có electron độc thân của nguyên tử clo


Thầy viet giup e lien ket cong hoá trị cua PCl5 được k ạ